约翰霍普金斯大学医学中心的研究人员报告说,一种最初开发用于治疗肾脏疾病的实验性药物可以延长小鼠的存活期并改善小鼠的肌肉功能,这些小鼠经过基因工程改造以发展为严重的杜氏肌营养不良症(DMD)。
根据肌肉萎缩症协会(MDA)的说法,DMD影响每5,000名活产男性中的1名,并由于缺乏一种称为肌营养不良蛋白的蛋白质而导致严重的肌肉萎缩和虚弱,这种蛋白质是增强肌肉细胞并保护它们免受机械损伤所必需的.肌营养不良蛋白基因位于X染色体中,因此DMD主要影响男孩。
只有当两条X染色体都受到影响时,女孩才会患上这种疾病。肌肉症状开始于2至4岁之间,到了十几岁时,大多数DMD患者无法行走。肌营养不良蛋白对心肌也很重要,因此心力衰竭经常发生在青少年后期到20岁出头。根据MDA,患有DMD的人通常活到20多岁或30岁出头。
没有治愈方法,但物理疗法和皮质类固醇可以减轻炎症,帮助延缓肌肉衰退,帮助缓解症状并提高生活质量。正在测试更新的基因靶向治疗,但它们仍然仅限于少数靶向患者。
这项于9月13日发表在JCIInsight上的新研究报告称,在患有严重DMD的小鼠中阻断名为TRPC6的离子通道的药物使它们的存活率增加了一倍,并改善了它们的骨骼肌和心肌功能。它还减少了与肌肉无力相关的骨骼畸形。
离子通道是主要存在于细胞外膜上的蛋白质组,它们的作用类似于孔,允许钙或钠等元素以受控方式进出细胞。TRPC6是这些蛋白质中的一种,主要允许钙进入细胞。
它被压力荷尔蒙和机械力激活,并被发现有助于钙异常进入缺乏肌营养不良蛋白的肌肉细胞。根据约翰霍普金斯大学医学院心脏病学教授、医学博士DavidKass和该研究的资深作者,这可能导致细胞损伤并最终导致细胞死亡。
“2014年,我的实验室首次表明,与正常细胞相比,当Duchenne小鼠拉伸时,进入心肌细胞的钙含量增加更多。这会导致节律异常。我们发现阻断TRPC6可以防止多余的钙进入心脏并减少心律失常”卡斯说。“我们认为长期的TRPC6阻滞剂可能有助于治疗这种综合征。不幸的是,我们当时使用的药物在细胞中效果很好,但在动物体内代谢过快,因此无法使用。”
在这项新研究中,研究人员使用了一种模拟人类严重疾病的DMD小鼠模型。老鼠的平均寿命为两个月(相当于人类的十几岁)。从出生后三天开始,研究人员用TRPC6抑制剂药物(BI749327,由Boehringer-IngelheimPharmaceuticals开发)或安慰剂治疗雄性和雌性DMD小鼠。接受安慰剂的小鼠中位生存率为4周,9周死亡率为100%。获得抑制剂的老鼠的寿命几乎翻了一番。
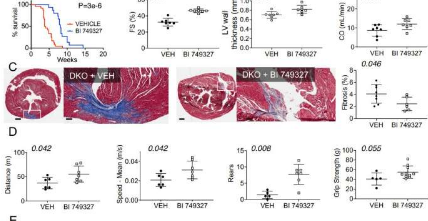
与未服用该药物的DMD小鼠相比,心脏功能改善了近50%,并且小鼠的运动速度提高了约50%。这些发现得到了另一项实验的支持,在该实验中,TRPC6被基因去除,因此DMD小鼠从未表达过这种蛋白质。他们还延长了寿命(几乎是对照组的三倍)并改善了肌肉功能。
“我们相信这可能是在这种非常严重的Duchenne模型中使用可以口服的化合物延长存活率的首批研究之一。虽然该分子不会恢复肌营养不良蛋白,但它会阻止另一种蛋白质的异常行为,这种行为是由缺乏抗肌萎缩蛋白,”卡斯说。“这不是杜兴的治愈方法,但如果人体试验复制了这些发现,这可能意味着患者可以存活到40多岁和50多岁,并有可能改善生活质量。”
根据肌肉萎缩症协会的数据,全球每年估计有20,000名儿童被诊断出患有杜兴氏症。
 东方时讯网
东方时讯网