研究人员为罕见的纤毛病开发基因疗法
美国国家眼科研究所(NEI)的研究人员开发了一种基因疗法,可以挽救受莱伯先天性黑蒙(LCA)影响的视网膜细胞纤毛缺陷,这种疾病会导致儿童早期失明。研究人员使用源自患者的视网膜类器官(也称为视网膜类器官)发现,由NPHP5(也称为IQCB1)基因突变引起的一种LCA会导致初级纤毛出现严重缺陷,这是一种结构几乎存在于身体的所有细胞中。这些发现不仅揭示了NPHP5蛋白在初级纤毛中的功能,而且还为这种致盲病症提供了潜在的治疗方法。NEI是美国国立卫生研究院的一部分。
该研究的首席研究员阿南德说:“看到小孩子因LCA早发而失明,真是太可悲了。NPHP5缺乏会导致早期失明,其形式较轻,在更严重的形式下,许多患者还表现出肾脏疾病和视网膜退化。”Swaroop博士,NEI神经生物学神经和修复实验室的高级研究员。“我们设计了一种基因治疗方法,可以帮助预防患有这种疾病的儿童失明,并且通过进一步的研究,它甚至可能有助于治疗这种疾病的其他影响。”
LCA是一种罕见的遗传疾病,会导致眼睛后部的感光视网膜退化。至少25个不同基因的缺陷可导致LCA。虽然对于一种形式的LCA有可用的基因治疗方法,但所有其他形式的疾病都没有治疗方法。NPHP5突变引起的LCA类型比较少见。它在所有情况下都会导致失明,在许多情况下还可能导致肾脏衰竭,这种情况称为Senior-Løken综合征。
三位博士后研究员KamilKruczek博士、ZepengQu博士和EmilyWelby博士与研究团队的其他成员一起从两名NPHP5缺乏症患者身上采集了干细胞样本。美国国立卫生研究院临床中心。这些干细胞样本用于生成视网膜类器官,即培养的组织簇,具有实际天然视网膜的许多结构和功能特征。源自患者的视网膜类器官特别有价值,因为它们密切模仿实际患者的基因型和视网膜疾病表现,并为测试治疗干预(包括基因疗法)提供“类人”组织环境。与患者一样,这些视网膜类器官在感光器中显示出缺陷,包括部分感光器称为“外段”。
在健康的视网膜中,光感受器外段包含称为视蛋白的光敏分子。当外部部分暴露在光线下时,感光器会启动一个神经信号,该信号传播到大脑并介导视觉。感光器外段是一种特殊类型的初级纤毛,这是一种几乎在所有动物细胞中都能找到的古老结构。
在健康的眼睛中,NPHP5蛋白被认为位于初级纤毛底部的门状结构,有助于过滤进入纤毛的蛋白质。先前对小鼠的研究表明,NPHP5与纤毛有关,但研究人员尚不清楚NPHP5在光感受器纤毛中的确切作用,也不清楚突变究竟如何影响蛋白质的功能。
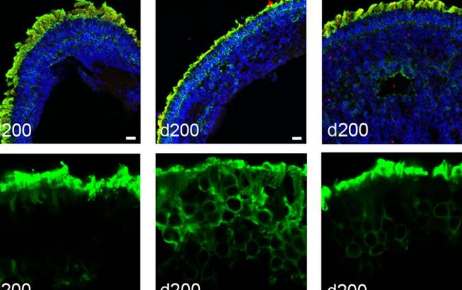
在本研究中,研究人员发现患者来源的视网膜类器官细胞中NPHP5蛋白水平降低,另一种称为CEP-290的蛋白质水平降低,该蛋白与NPHP5相互作用并形成初级纤毛门。(CEP-290中的突变构成LCA的最常见原因。)此外,视网膜类器官中的光感受器外段完全缺失,而本应定位于外段的视蛋白却在光感受器细胞体的其他地方发现.
当研究人员引入含有NPHP5功能版本的腺相关病毒(AAV)载体作为基因治疗载体时,视网膜类器官显示出集中在外段适当位置的视蛋白显着恢复。研究结果还表明,功能性NPHP5可能稳定了初级纤毛门。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
宝子们,杭州 房子装修完成啦!这次要给大家分享几家设计超赞的装修公司哦。它们各具特色,从空间规划到风格...浏览全文>>
-
欲筑室者,先治其基。在上海,装修房子对于每个业主而言,都是极为关键的一步,然而,如何挑选一家值得信赖的...浏览全文>>
-
2025年以来,联通支付严格贯彻落实国家战略部署,以数字和科技为驱动,做好金融五篇大文章,履行支付为民社会...浏览全文>>
-
良工巧匠,方能筑就华居;精雕细琢,方可打造美家。当我们谈论装修公司时,选择一家靠谱可靠的公司是至关重要...浏览全文>>
-
在当今社会,随着城市化进程的高速推进,建筑垃圾的产生量与日俱增。据权威数据显示,我国每年建筑垃圾产生量超 ...浏览全文>>
-
家人们,在上海要装修,选对公司那可太重要了!古语有云:"安得广厦千万间,大庇天下寒士俱欢颜。"一个温馨的...浏览全文>>
-
近年来,新能源汽车市场发展迅猛,各大品牌纷纷推出各具特色的车型以满足消费者多样化的需求。作为国内新能源...浏览全文>>
-
近年来,随着汽车市场的不断变化和消费者需求的升级,安徽滁州地区的宝来2025新款车型在市场上引起了广泛关注...浏览全文>>
-
随着汽车市场的不断变化,滁州地区的消费者对高尔夫车型的关注度持续上升。作为大众品牌旗下的经典车型,高尔...浏览全文>>
-
在2023年,大众探影以其时尚的设计和出色的性能赢得了众多消费者的青睐。作为一款小型SUV,探影凭借其紧凑的车...浏览全文>>
- 安徽滁州途安L新车报价2022款,最低售价16.68万起,入手正当时
- 小鹏G7试驾,新手必知的详细步骤
- 别克GL8预约试驾,4S店的贴心服务与流程
- 安徽阜阳ID.4 CROZZ落地价全解,买车必看的省钱秘籍
- 淮北探岳多少钱 2025款落地价,最低售价17.69万起现在该入手吗?
- 安徽淮南大众CC新款价格2025款多少钱能落地?
- 淮北长安启源C798价格,最低售价12.98万起现在该入手吗?
- 安徽淮南途锐价格,各配置车型售价全解析
- 蒙迪欧试驾预约,4S店体验全攻略
- 沃尔沃XC40试驾需要注意什么
- 滁州ID.4 X新车报价2025款,各车型售价大公开,性价比爆棚
- 试驾思域,快速操作,轻松体验驾驶乐趣
- 试驾长安CS35PLUS,一键搞定,开启豪华驾驶之旅
- 天津滨海ID.6 X落地价限时特惠,最低售价25.9888万起,错过不再有
- 天津滨海凌渡多少钱?看完这篇购车攻略再做决定
- 安徽池州长安猎手K50落地价,买车前的全方位指南
- 山东济南ID.6 CROZZ 2024新款价格,最低售价19.59万起,现车充足
- 试驾海狮05EV,新手必知的详细步骤
- 生活家PHEV多少钱 2025款落地价走势,近一个月最低售价63.98万起,性价比凸显
- 奇瑞风云A9试驾,新手必知的详细步骤
