蛋白介导,它负责约70%的胆固醇吸收。NPC1L1缺陷小鼠对饮食诱导的高胆固醇血症具有抵抗力,这为通过抑制NPC1L1表达或活性来干预相关疾病提供了令人信服的策略。
NPC1L1蛋白在小肠的刷状缘膜中表达。该蛋白质广泛N-糖基化,由1332个氨基酸和13个跨膜片段组成,这使得很难制备理想的抗体来分析其体内行为。基于体外细胞系的研究,推测NPC1L1通过网格蛋白介导的内吞作用介导胆固醇吸收。然而,这个概念也有一些未解决的挑战。实际上,NPC1L1与胆固醇的内吞囊泡尚未在生理条件下得到证实,因为没有可行的工具来可视化和评估NPC1L1囊泡在体内的内吞作用。
中国海军军医大学的科学家利用CRISPR/Cas9基因编辑技术构建了一种小鼠模型,其中内源性NPC1L1蛋白被标记有增强型绿色荧光蛋白(EGFP)。NPC1L1-EGFP小鼠使研究人员能够通过荧光观察和评估NPC1L1-cago在肠道胆固醇吸收过程中的囊泡内吞作用。这项研究在线发表在《生命新陈代谢》杂志上。
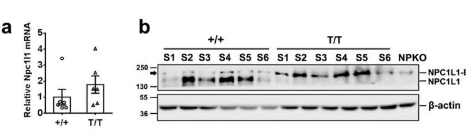
在这项研究中,发现纯合NPC1L1-EGFP敲入小鼠在“食物”或高胆固醇饮食条件下具有正常的胆固醇稳态。NPC1L1-EGFP融合蛋白的荧光定位于绒毛的刷状缘膜,而不是十二指肠、空肠和回肠中的隐窝,而不是结肠中的隐窝。该模式与对照小鼠中内源性NPC1L1分布的特征一致。早在5分钟内,EGFP阳性囊泡就在刷状缘膜下方可见,并在胆固醇口服灌胃后15分钟达到峰值。
值得注意的是,囊泡与早期内体标记物EEA1和菲律宾染色的游离胆固醇共定位,灌胃胆固醇引发EEA1阳性囊泡在刷状缘膜下的积累。用NPC1L1抑制剂依折麦布预处理可抑制这些胆固醇诱导的内吞囊泡的形成,进一步支持囊泡内吞作用参与NPC1L1介导的胆固醇吸收。
这项研究首次清楚地证明了在生理条件下肠道胆固醇吸收过程中NPC1L1内吞小泡中的游离胆固醇。它提供了一个可行的工具来评估NPC1L1货物的囊泡内吞作用以及在病理生理和药理学条件下体内的胆固醇吸收,并可用于药物发现。
此外,鉴于NPC1L1还介导非胆固醇甾醇(如植物甾醇和生育酚)的肠道吸收,该小鼠模型也有利于谷甾醇血症和维生素E缺乏症领域的研究人员。
 东方时讯网
东方时讯网