碳水化合物研究人员不断努力克服的主要障碍之一是可用于破译糖类作用的工具有限。作为一种解决方法,大多数研究人员使用从植物或真菌中分离出来的凝集素(糖结合蛋白),但它们体积大,结合力弱,而且它们的特异性和检测到的糖的范围有限。
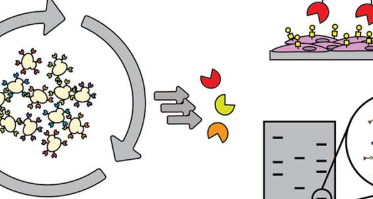
在ACSChemicalBiology上发表的一项新研究中,BarbaraImperiali教授小组的研究人员开发了一个平台来解决这一缺点。
“碳水化合物聚合物的挑战在于它们的生物合成不是模板驱动的,”该研究的资深作者、化学和生物学系教授Imperiali说。“生物学、医学和生物技术一直受到蛋白质和核酸技术进步的推动。碳水化合物领域非常落后,正在拼命寻找工具。”
识别碳水化合物结合蛋白
碳水化合物的生物合成需要单个糖分子之间的每一个连接都由一种特定的酶来完成,而且还没有现成的方法来破译复杂碳水化合物的结构和序列。可以产生针对碳水化合物的抗体,但这样做具有挑战性、成本高,并且会产生比研究真正需要的分子大得多的分子。
这个受有限机制困扰的领域的理想资源是发现大小有限的结合蛋白,这些蛋白可以识别小块碳水化合物,通过使用这些粘合剂拼凑出一个结构,或者是检测和识别复杂结构中特定碳水化合物的方法。
这项研究的作者使用定向进化和巧妙的筛选设计,从完全没有结合碳水化合物能力的蛋白质中识别碳水化合物结合蛋白。他们的发现为识别具有多样性和可编程特异性的碳水化合物结合蛋白奠定了基础。
简化协作
这一进步将使研究人员能够追踪用户定义的糖目标,而不受凝集素作用的限制,也不受产生抗体能力的挑战。这些结果可能有助于激发未来与工程界的合作,以最大限度地提高糖生物学酵母表面展示管道的效率。事实上,这条管道适用于蛋白质,但糖类是更困难的目标,需要修改管道。
就未来的应用而言,这项创新的潜力从诊断到长期的治疗,并为与麻省理工学院及其他研究人员的合作铺平了道路。例如,化学教授劳拉·基斯林(LauraKiessling)的研究小组与结核分枝杆菌(Mtb)合作,它具有不寻常的细胞壁组成,具有独特、独特和专有的糖分。使用这种方法,活页夹可能会演变成Mtb上的特定功能。
化学工程教授HadleySikes开发了基于纸张的诊断工具,其中放置了特定表位或标记的结合伙伴,并且利用这一发现,从长远来看,可以开发出横向流动分析装置。
为未来的解决方案奠定基础
在癌症中,某些糖在细胞表面的表达过多,因此从理论上讲,研究人员可以利用这一发现(也适用于标记)来开发一种利用进化的聚糖结合物进行检测的工具。
这一发现也将为改善细胞成像做出重大贡献。研究人员可以使用简单的连接策略用荧光团修饰结合物,然后可以选择最适合组织或细胞成像的荧光团。例如,Kiessling小组可以应用用荧光团标记的小蛋白结合物来检测细菌糖,从而启动荧光激活细胞分选以探测复杂的微生物混合物。
这反过来又可以用来确定患者的微生物组是如何受到干扰的。它还有可能使用这些类型的试剂来筛查患者口腔或其上消化道或下消化道的微生物组,以读出社区内的不平衡情况。在更遥远的未来,粘合剂可能具有治疗目的,例如根据细菌显示的糖清除特定细菌的胃肠道或口腔。
 东方时讯网
东方时讯网