尽管化学疗法可以挽救生命,但癌症治疗常常使患者遭受令人衰弱的副作用,包括处理速度、记忆力、执行功能和注意力方面的认知障碍。这些被称为“化疗脑”的挥之不去的症状会在患者完成癌症治疗后很长时间内显着影响他们的生活质量。
目前,没有FDA批准的药物来减轻这些缺陷。在突破性发现中,著名的圣路易斯大学疼痛研究员DanielaSalvemini博士和她的团队发现了化疗药物导致这些缺陷时发生的一些分子事件。更有希望的是,他们发现一种已经批准用于治疗多发性硬化症的FDA药物似乎也可以减少与化疗相关的认知障碍(CRCI)。
日益增长的需求
国家癌症研究所(NCI)预计到2029年癌症存活率将达到21.700万。随着存活率的提高,解决化疗严重、持久的神经毒性副作用的需要正在增加。
CRCI是化疗的主要神经毒性副作用,影响超过50%接受广泛使用的化疗药物治疗的患者,包括紫杉类药物如紫杉醇和铂类药物如顺铂。这些药物被广泛用作多种癌症的标准治疗的一部分,包括头颈癌、睾丸癌、结肠癌、乳腺癌、卵巢癌和非小细胞肺癌。
当通过神经心理学测试进行评估时,高达75%的接受化疗治疗神经系统以外癌症的患者报告了认知缺陷。
Salvemini是WilliamBeaumont药理学和生理学教授兼圣路易斯大学系主任,他说CRCI深刻影响患者的生活质量。
“由于CRCI的多因素起源,我们目前对CRCI潜在机制及其对认知影响的理解有限,”SLU亨利和阿米莉亚纳斯鲁拉神经科学中心主任、圣路易斯研究员Salvemini说科学院。“更好地了解这些机制对于开发新疗法和提高幸存者的生活质量至关重要。”
新发现
在她于2022年9月1日发表在《临床研究杂志》上的最新论文“中枢神经系统中的鞘氨醇1-磷酸受体1激活驱动顺铂诱导的认知障碍”中,Salvemini和她的团队提出了第一个证据化学疗法改变了与认知功能相关的大脑关键区域中称为鞘脂代谢的重要细胞途径。
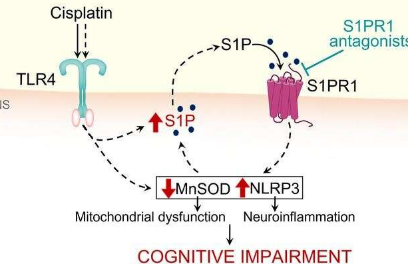
Salvemini指出,在中枢神经系统中,顺铂增加了强效信号分子1-磷酸鞘氨醇(S1P)的水平,这通过激活星形胶质细胞上的S1P受体亚型1(S1PR1)和S1PR1驱动的线粒体来促进CRCI的发展功能障碍和神经炎症过程。她说,从机制上讲,该团队揭示了顺铂诱导的S1P形成是由toll样受体4介导的。
他们的发现弥补了理解CRCI分子机制的空白,并确定了一个新的目标,用于使用功能性S1PR1拮抗剂进行治疗干预。重要的是,S1PR1拮抗剂不会干扰化疗的疗效,正如他们和其他人在之前的工作中所展示的那样,并且还可以阻断肿瘤细胞的生长、炎症和转移。
“我们的研究结果令人着迷,因为两种功能性S1PR1拮抗剂已经被FDA批准用于治疗多发性硬化症,”Salvemini说。“重新利用这些药物来预防CRCI将是提高癌症治疗患者生活质量的突破性转变。”
在之前的研究中,Salvemini开创了一种治疗神经性疼痛的研究,该研究可以为无效的类固醇和成瘾的阿片类药物提供第一个替代方案。Salvemini实验室的工作证实,中枢神经系统中S1PR1信号传导的改变对化疗的反应也有助于化疗引起的神经性疼痛,这是癌症治疗的另一种中枢神经毒性。这项工作推动了两项正在进行的NCI临床试验,以测试被批准用于治疗多发性硬化症的药物Gilenya的潜在用途,以预防接受紫杉醇治疗的乳腺癌患者的神经性疼痛。
“我们的工作非常具有转化性,”Salvemini说。“我们试图在分子水平上了解这些机制,确定目标,与我们的化学家合作,制造针对该特定途径的新药,对其进行测试,然后采取必要的步骤沿着该化合物前进,直到它准备好在临床试验中研究。”
 东方时讯网
东方时讯网